Если вы когда-нибудь видели голубоватый цвет на пенни, скорее всего, это ацетат меди. Эти мелкие синие кристаллы ацетата меди образуются, когда медь реагирует с уксусной кислотой. Вы можете создать ацетат меди в лабораторных условиях или дома. Для создания этого химического вещества вам не потребуется много научных знаний или доступ к дорогостоящему лабораторному оборудованию.
Шаги
Метод 1 из 3: приготовление раствора ацетата меди из бытовой химии

Шаг 1. Смешайте уксусную кислоту и перекись водорода
Бытовой вариант уксусной кислоты - уксус. Это разбавленная форма уксусной кислоты, которая обнаруживается во многих домашних химических экспериментах. Смешайте его с перекисью водорода, которую обычно хранят дома для очистки порезов и царапин (в коричневой пластиковой бутылке). Используйте смесь 50/50.
- Например, если вы используете 1 стакан (237 мл) уксуса, используйте 1 стакан (237 мл) перекиси водорода.
- Лучше всего использовать простой белый уксус.
- При работе с кислотами и окислителями надевайте перчатки и защитные очки. Вы не хотите, чтобы они попали на вашу кожу или в глаза.

Шаг 2. Нагрейте раствор в стеклянной посуде
Хотя раствор не обязательно должен кипеть, чтобы реакция произошла, доведение его до кипения избавляет от догадок. Положите раствор на плиту в стеклянную емкость, пригодную для использования в плите, и дайте ему слегка закипеть. После кипения он готов вступить в реакцию с медью с образованием ацетата меди.

Шаг 3. Добавьте в раствор медь
Используйте медную проволоку или пенни, чтобы подать медь для реакции. Опустите медь в раствор, стараясь не разбрызгаться и не прикоснуться к горячему раствору. Вы должны быть в перчатках и защитных очках на случай, если раствор разбрызгается.
Если вы используете пенни, знайте, что вы должны использовать только пенни, отчеканенные в 1982 году или ранее. После этого пенни делали из цинка с медным покрытием и содержали только около 2,5% меди (по сравнению с 88-95% меди до 1982 года).

Шаг 4. Наблюдайте за реакцией
Следите за изменением цвета раствора. Синий цвет указывает на образование ацетата меди. Это должно произойти в считанные минуты.
Если раствор не станет синим, ацетат меди не образовался. В этом случае проверьте свои реагенты. Убедитесь, что уксус и перекись находятся в правильном соотношении, а срок годности химикатов не истек. Кроме того, убедитесь, что ваш медный источник действительно медный, а не просто другой металл, покрытый медью
Метод 2 из 3: Реакция обычных химических веществ с образованием раствора ацетата меди
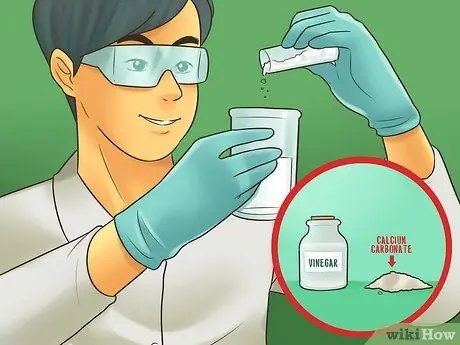
Шаг 1. Сделайте ацетат кальция
Добавьте карбонат кальция в уксус. Перемешивайте до полного растворения карбоната кальция. Карбонат кальция можно заказать у поставщика химикатов, но в этом нет необходимости, поскольку он является основным ингредиентом мела.
- Используйте простой белый уксус.
- Вы можете просто измельчить мел, чтобы получить порошок карбоната кальция.
- При работе с кислотами следует пользоваться защитными очками и перчатками.
- По объему используйте вдвое меньше карбоната кальция, чем уксуса. Например, если вы используете 2 стакана (473 мл) уксуса, используйте 1 стакан (237 мл) карбоната кальция.
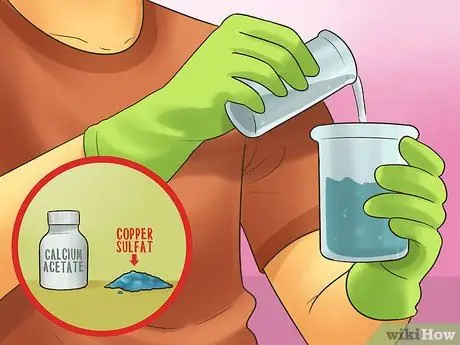
Шаг 2. Добавьте ацетат кальция в раствор сульфата меди
Сульфат меди - еще одно химическое вещество, которое легко найти в магазине для дома и сада. Его часто называют фунгицидом. Его также могут назвать убийцей пней. Он растворен в воде.
- Медленно вливайте раствор ацетата кальция, пока цвет не станет синим. Синий цвет указывает на то, что вы получили ацетат меди.
- Полученный раствор должен быть синего цвета.
- Избегайте попадания раствора на кожу или в глаза, надевая перчатки и защитные очки.

Шаг 3. Отфильтруйте раствор
Синий раствор содержит растворенный ацетат меди. Также будет твердое вещество, которое выпадет в осадок из раствора (сульфат кальция). Вылейте раствор через ситечко, чтобы удалить сульфат кальция. У вас останется синий раствор ацетата меди.
- Сульфат кальция раздражает кожу и глаза, поэтому при работе с ним надевайте защитные очки и перчатки. При попадании на кожу немедленно смойте водой с мылом. Если он попал в глаза, промойте их теплой водой не менее 15 минут.
- Вы можете безопасно утилизировать небольшое количество сульфата кальция (менее 5 фунтов или 2,3 кг) в обычном контейнере для мусора, если контейнер находится в хорошем состоянии и имеет плотно закрывающуюся крышку.
- Подумайте о том, чтобы сохранить сульфат кальция, чтобы использовать его в других экспериментах, например, при нагревании древесным углем для получения сульфида кальция.
Метод 3 из 3: выращивание кристаллов ацетата меди

Шаг 1. Растворите моногидрат ацетата меди в воде
Эти гранулы можно найти в магазине химикатов или заказать через Интернет. Опустите их в теплую воду. Размешайте воду стеклянной палочкой для перемешивания до полного растворения кристаллов. Раствор должен быть синего цвета.
Если вы сами приготовили раствор ацетата меди из бытовой химии, в этом шаге нет необходимости

Шаг 2. Облегчить выпадение осадков
Самопроизвольно выпадает ацетат меди. Оставьте раствор в сухом прохладном месте. По мере испарения воды ацетат меди будет вытеснен из раствора. Вы увидите, как на поверхности блюда образуются синие кристаллы.
- Вы также можете бросить кристалл в раствор, чтобы ускорить осаждение.
- Храните раствор в недоступном для маленьких детей и домашних животных месте. Если оставить без присмотра, домашние животные и маленькие дети могут проглотить раствор. Это может привести к острому отравлению медью, которое может быть опасным или даже смертельным.

Шаг 3. Высушите кристаллы
Получив кристаллы, слейте оставшийся раствор. Переложите кристаллы на бумажное полотенце. Дайте им посидеть день или два, чтобы они высохли.
подсказки
Если после растворения моногидрата ацетата меди в растворе появился твердый слой, добавьте немного уксуса, чтобы растворить его
Предупреждения
- Всегда надевайте перчатки при работе с химическими веществами.
- Храните раствор в недоступном для маленьких детей и домашних животных месте. Не употребляйте раствор.
- При работе с химическими веществами всегда надевайте защитные очки.
