Все основные элементы состоят из электронов, протонов и нейтронов. Электрон - это отрицательно заряженная частица, составляющая часть атома. Фундаментальное понятие в химии - это способность определять, сколько электронов содержит атом. Это можно легко определить с помощью периодической таблицы элементов. Другие важные концепции включают в себя то, как найти количество нейтронов и валентных электронов (количество электронов в его внешней оболочке) в элементе.
Шаги
Метод 1 из 2: определение числа электронов в нейтральных атомах
Шаг 1. Получите периодическую таблицу элементов
Это таблица с цветовой кодировкой, в которой все известные элементы упорядочены по атомной структуре. Каждый элемент имеет аббревиатуру из 1, 2 или 3 букв и указывается вместе с его атомным весом и атомным номером.
Периодические таблицы можно легко найти в книгах по химии, а также в Интернете
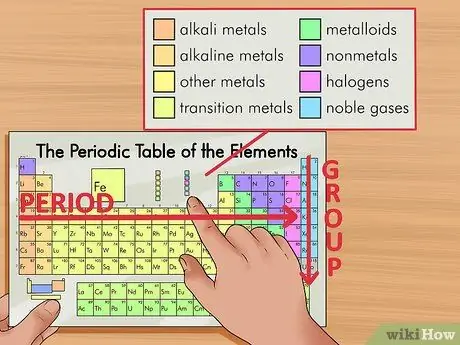
Шаг 2. Найдите нужный элемент в периодической таблице
Элементы упорядочены по атомным номерам и разделены на три основные группы: металлы, неметаллы и металлоиды (полуметаллы). Далее они подразделяются на семейства, включая щелочные металлы, галогены и благородные газы. Каждый столбец таблицы называется группой, а каждая строка - периодом.
- Если вы знаете детали своего элемента, например, в какой группе или периоде он находится, его будет легче найти.
- Если вы ничего не знаете о рассматриваемом элементе, просто ищите в таблице его символ, пока не найдете его.
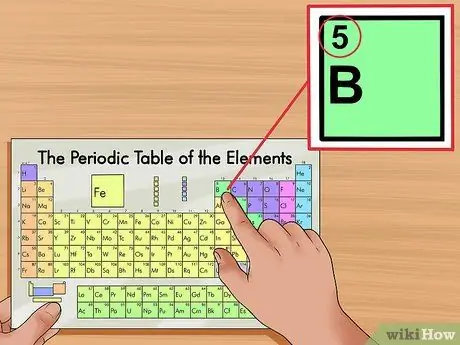
Шаг 3. Найдите атомный номер элемента
Атомный номер отображается в верхнем левом углу или по центру над символом элемента в квадрате. Атомный номер определяет количество протонов, присутствующих в этом конкретном элементе. Протоны - это частицы элемента, обеспечивающие положительный заряд. Поскольку электроны заряжены отрицательно, когда элемент находится в нейтральном состоянии, у него будет такое же количество протонов, как и у электронов.
Например, бор (B) имеет атомный номер 5, что означает, что он имеет 5 протонов и 5 электронов
Метод 2 из 2: Определение электронного числа положительно / отрицательно заряженных ионов
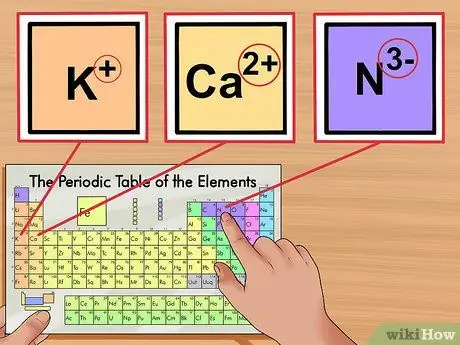
Шаг 1. Определите заряд иона
Добавление и удаление электронов в атоме не изменяет его идентичность, но меняет его заряд. В этих случаях теперь у вас есть ион, например K+, Ca2+, или N3-. Обычно заряд указывается в верхнем индексе справа от аббревиатуры атома.
- Поскольку электрон имеет отрицательный заряд, когда вы добавляете дополнительные электроны, ион становится более отрицательным.
- Когда вы удаляете электроны, ион становится более положительным.
- Например, N3- имеет заряд -3, а Ca2+ имеет заряд +2.

Шаг 2. Вычтите заряд из атомного номера, если ион положительный
Если заряд положительный, ион потерял электроны. Чтобы определить, сколько электронов осталось, вычтите количество заряда из атомного номера. В этом случае протонов больше, чем электронов.
Например, Ca2+ имеет заряд +2, следовательно, у него на 2 электрона меньше, чем у нейтрального атома кальция. Атомный номер кальция 20, следовательно, у этого иона 18 электронов.

Шаг 3. Добавьте заряд к атомному номеру, если заряд отрицательный
Если заряд отрицательный, ион получил электроны. Чтобы определить общее количество электронов, добавьте количество заряда к атомному номеру. В этом случае протонов меньше, чем электронов.
