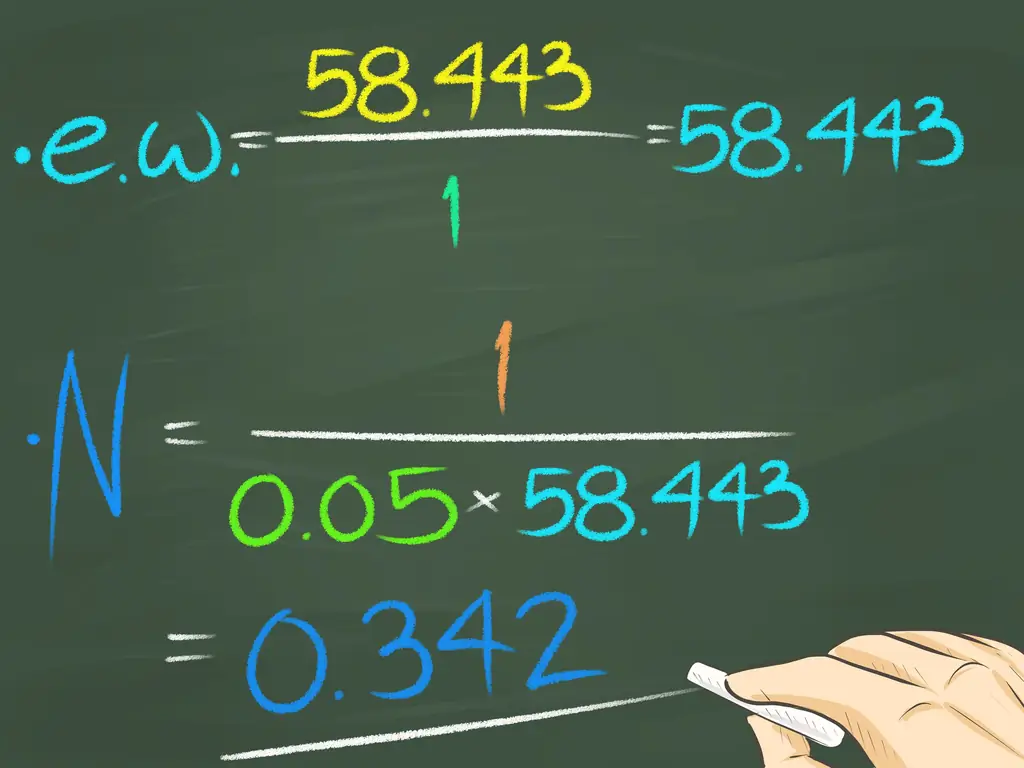Многие химические вещества доступны в растворенной жидкой форме, а не в твердой форме. Жидкие химические вещества легче дозировать и измерять, чем твердые, тем более что твердые химические вещества обычно представляют собой порошок. Однако стехиометрия химических реакций усложняется из-за способа доставки жидкости. Стехиометрия выполняет вычисления с использованием количества желаемого вещества, помещенного в уравнения. Жидкость, используемая для растворения вещества, не будет участвовать в реакции, и стехиометрия не будет учитывать эту жидкость в реакции. Количество доставляемого реагирующего вещества может быть определено путем определения нормальности раствора. Воспользуйтесь этими советами, чтобы узнать, как рассчитать нормальность.
Шаги

Шаг 1. Соберите информацию об эквивалентной массе реагирующего вещества
Обратитесь к справочникам по химическим веществам, чтобы узнать валентность и молекулярную массу вещества. Молекулярная масса - это отношение массы 1 молекулы вещества к массе (одна молекула углерода12 делится на 12.) Валентность определяется максимальным числом субатомных валентных связей или связей между атомами, которые вещество может образовывать с другими веществами. Эта информация потребуется для определения нормальности.

Шаг 2. Определите эквивалентный вес вещества
Эквивалентная масса вещества равна молекулярной массе, деленной на валентность.
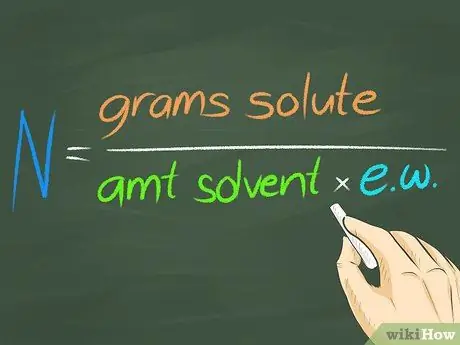
Шаг 3. Рассчитайте нормальность
Нормальность - это концентрация исследуемого вещества в растворяющейся жидкости. Следовательно, нормальность является свойством смеси и будет варьироваться в зависимости от использования более или менее растворяющей жидкости для помещения интересующего вещества в раствор. Нормальность - это количество граммов исследуемого вещества, деленное на (эквивалентный вес вещества, умноженный на количество растворяющейся жидкости).
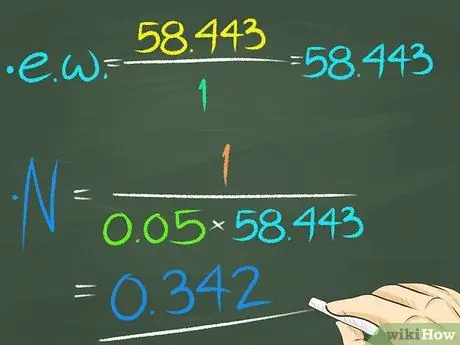
Шаг 4. Попробуйте пример
Растворите хлорид натрия (NaCl) в воде. Хлорид натрия имеет валентность 1 и молекулярную массу 58,443. Следовательно, эквивалентный вес составляет 58,443 / 1 или 58,443. 1 грамм NaCl растворяют в 0,05 л воды, поэтому нормальность раствора составляет 1 / (58,443 x 0,05) или 0,342.