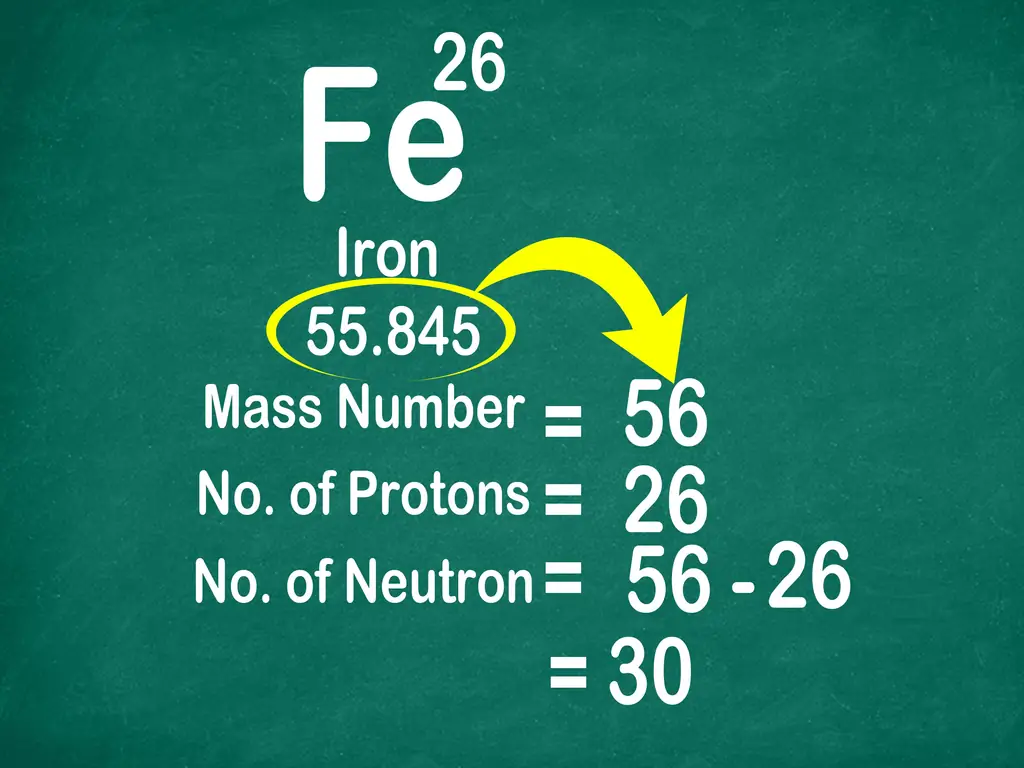Если вы находите таблицу Менделеева непонятной и сложной для понимания, вы не одиноки! Понять, как это работает, может быть сложно, но умение читать поможет вам добиться успеха в науке. Начните с распознавания структуры периодической таблицы и того, что она говорит вам о каждом элементе. Далее вы можете изучить каждый элемент. Наконец, используйте информацию, представленную в периодической таблице, чтобы найти количество нейтронов в атоме.
Шаги
Образец периодической таблицы
Образец периодической таблицы
Поддержка wikiHow и разблокировать все образцы.
Часть 1 из 3: Распознавание структуры Периодической таблицы
Шаг 1. Прочтите таблицу Менделеева слева направо
Элементы упорядочены по их атомным номерам, которые увеличиваются по мере того, как вы перемещаетесь по таблице Менделеева и вниз. Атомный номер - это количество протонов в атоме элемента. Вы также заметите, что атомная масса каждого элемента увеличивается по мере того, как вы перемещаетесь по столу. Это означает, что вы можете многое узнать о весе элемента, просто взглянув на его место на столе.
- Атомная масса увеличивается по мере того, как вы перемещаетесь по таблице или вниз, потому что масса рассчитывается путем сложения протонов и нейтронов в атоме каждого элемента. Количество протонов увеличивается с каждым элементом, а значит, увеличивается и вес.
- Электроны не входят в атомную массу, поскольку они вносят гораздо меньший вклад в вес атома, чем протоны и нейтроны.
Шаг 2. Обратите внимание, что каждый элемент содержит на 1 протон больше, чем его предшественник
Вы можете сказать это, посмотрев на атомный номер. Атомные номера расположены слева направо. Поскольку элементы также расположены по группам, вы увидите пробелы в таблице.
Например, первая строка содержит водород с атомным номером 1 и гелий с атомным номером 2. Однако они находятся на противоположных концах таблицы, поскольку находятся в разных группах
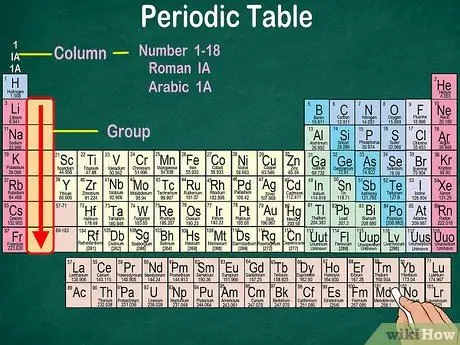
Шаг 3. Распознайте группы, имеющие общие физические и химические свойства
Группы, также известные как семьи, помещаются в вертикальный столбец. В большинстве случаев группы также будут одного цвета. Это поможет вам определить, какие элементы имеют схожие физические и химические свойства друг с другом, что позволит вам предсказать, как они будут себя вести. Каждый элемент в определенной группе имеет одинаковое количество электронов на своей внешней орбитали.
- Большинство элементов попадают в 1 группу, но водород можно отнести к семейству галогенов или щелочных металлов. На некоторых графиках он будет отображаться с обоими.
- В большинстве случаев столбцы будут пронумерованы от 1 до 18, над или под таблицей. Цифры могут быть показаны римскими цифрами (IA), арабскими цифрами (1A) или цифрами (1).
- Когда вы спускаетесь по группе сверху вниз, это называется «чтение группы вниз».
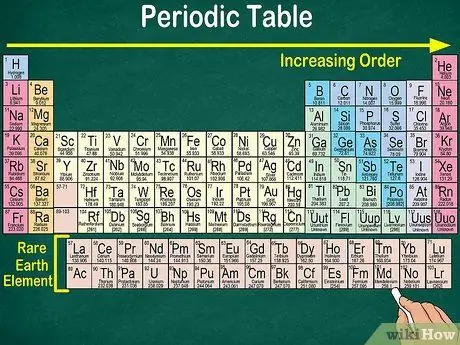
Шаг 4. Обратите внимание, почему в таблице есть пробелы
Хотя элементы упорядочены на основе их атомных номеров, они также организованы в группы и семейства, которые обладают одинаковыми физическими и химическими свойствами. Это поможет вам лучше понять, как ведет себя каждый элемент. Поскольку элементы не всегда аккуратно распределяются по группам по мере увеличения их числа, в периодической таблице есть пробелы.
- Например, в первых трех строках есть пробелы, поскольку переходные металлы не появляются в таблице до атомного номера 21.
- Точно так же элементы с 57 по 71, которые являются редкоземельными элементами, обычно изображаются как подмножество в правом нижнем углу таблицы.
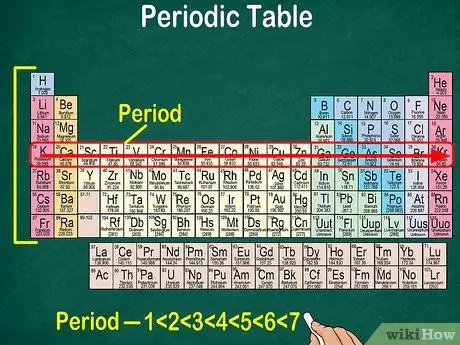
Шаг 5. Обратите внимание, что каждая строка называется точкой
Все элементы в периоде имеют одинаковое количество атомных орбиталей, по которым идут их электроны. Количество орбиталей будет соответствовать номеру периода. Всего 7 рядов, то есть 7 периодов.
- Например, элементы периода 1 имеют 1 орбиталь, а элементы периода 7 имеют 7 орбиталей.
- В большинстве случаев они пронумерованы от 1 до 7 в левой части таблицы.
- Когда вы перемещаетесь по строке слева направо, это называется «чтением за период».
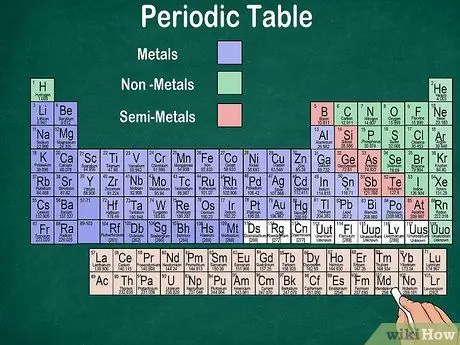
Шаг 6. Различайте металлы, полуметаллы и неметаллы
Вы можете лучше понять свойства элемента, узнав, к какому типу он относится. К счастью, в большинстве периодических таблиц цвет используется для обозначения того, является ли элемент металлическим, полуметаллическим или неметаллическим. Вы заметите, что металлы находятся слева от таблицы, а неметаллы - справа. Между ними зажаты полуметаллы.
- Имейте в виду, что водород может быть сгруппирован как с галогенами, так и с щелочными металлами из-за его свойств, поэтому он может отображаться с обеих сторон таблицы или может быть окрашен по-разному.
- Элементы маркируются как металлические, если они имеют блеск, твердые при комнатной температуре, проводят тепло и электричество, а также являются пластичными и пластичными.
- Элементы считаются неметаллами, если им не хватает блеска, они не проводят тепло или электричество и не податливы. Эти элементы обычно представляют собой газы при комнатной температуре, но также могут становиться твердыми или жидкими при определенных температурах.
- Элементы обозначаются как полуметаллы, если они обладают сочетанием свойств металлов и неметаллов.
Часть 2 из 3: изучение элементов
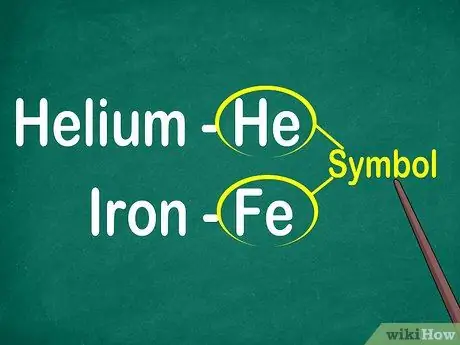
Шаг 1. Распознайте 1-2-буквенный символ элемента
Чаще всего он отображается в центре поля крупным шрифтом. Этот символ сокращает имя элемента, которое стандартизировано для разных языков. Когда вы проводите эксперименты или работаете с уравнениями элементов, вы, скорее всего, будете использовать символы элементов, поэтому важно ознакомиться с ними.
Этот символ обычно происходит от латинской формы имени элемента, но может быть производным от общепринятого общепринятого имени, особенно для новых элементов. Например, символ гелия - He, что очень похоже на обычное имя. Однако символ железа - Fe, который поначалу распознать труднее

Шаг 2. Найдите полное имя элемента, если оно есть
Это имя элемента, которое вы будете использовать при его написании. Например, «Гелий» и «Углерод» - названия элементов. В большинстве случаев он появляется сразу под символом, но его расположение может варьироваться.
В некоторых таблицах Менделеева полное название может быть опущено с использованием только символа
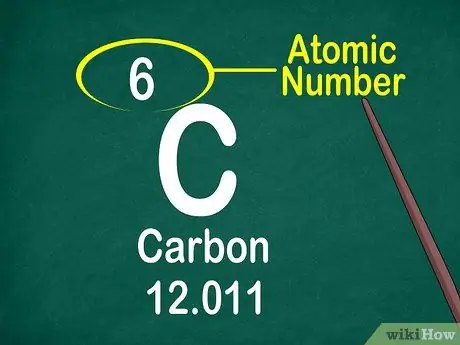
Шаг 3. Найдите атомный номер
Атомный номер часто находится вверху коробки, в центре или в углу. Однако он может располагаться под символом или именем элемента. Атомные номера идут последовательно от 1 до 118.
Атомный номер будет целым числом, а не десятичным
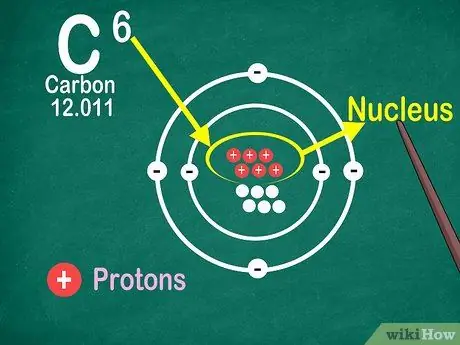
Шаг 4. Определите, что атомный номер - это количество протонов в атоме
Все атомы элемента содержат одинаковое количество протонов. В отличие от электронов, атом не может получать или терять протоны. В противном случае элемент изменился бы!
Вы также будете использовать атомный номер, чтобы найти количество электронов и нейтронов
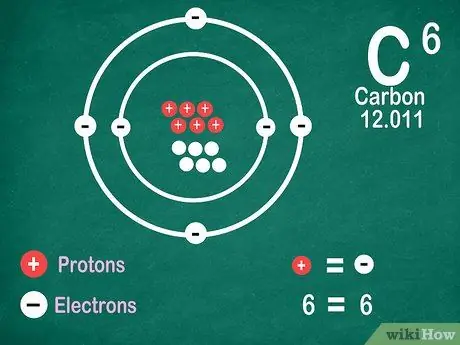
Шаг 5. Знайте, что элементы содержат такое же количество электронов, что и протоны
Есть исключение, если они ионизированы. Протоны имеют положительный заряд, а электроны - отрицательный. Поскольку обычные атомы не имеют электрического заряда, это означает, что электроны и протоны равны. Однако атом может терять или приобретать электроны, что делает его ионизированным.
- Ионы электрически заряжены. Если у иона больше протонов, он положительный, что обозначается положительным знаком рядом с символом иона. Если у него больше электронов, ион отрицательный, что обозначается отрицательным символом.
- Вы не увидите символа плюса или минуса, если элемент не ион.
Часть 3 из 3: Использование атомного веса для расчета нейтронов

Шаг 1. Найдите атомный вес
Атомный вес обычно отображается внизу поля под символом элемента. Атомный вес представляет собой общий вес частиц в ядре, который включает протоны и нейтроны. Однако ионы усложняют расчет, поэтому атомный вес представляет собой среднее значение атомной массы элемента и атомной массы его ионов.
- Поскольку веса являются усредненными, большинство элементов будут иметь атомные веса с десятичными знаками.
- Хотя может показаться, что атомный вес увеличивается в количестве от верхнего левого угла до нижнего правого угла, это не так во всех случаях.
Шаг 2. Определите массовое число изучаемого элемента
Вы можете найти массовое число, округлив атомную массу до ближайшего целого числа. Это объясняет тот факт, что атомный вес представляет собой среднее значение всех возможных атомных масс для этого элемента, включая ионы.
Например, атомный вес углерода составляет 12,011, что округляется до 12. Точно так же вес железа составляет 55,847, что округляется до 56
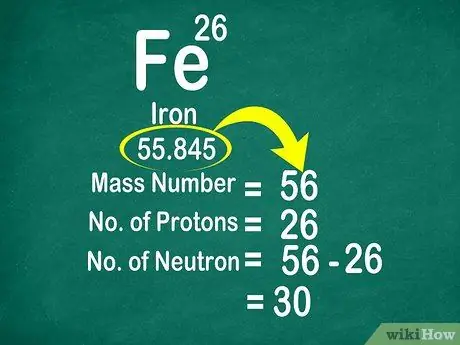
Шаг 3. Вычтите атомный номер из массового числа, чтобы найти нейтроны
Массовое число рассчитывается путем сложения количества протонов и нейтронов. Это позволяет вам легко найти количество нейтронов в атоме, вычитая количество протонов из массового числа!
- Используйте эту формулу: нейтроны = массовое число - протоны.
- Например, массовое число углерода равно 12, и у него 6 протонов. Поскольку 12-6 = 6, вы знаете, что у углерода 6 нейтронов.
- Другой пример: массовое число железа 56 и 26 протонов. Поскольку 56 - 26 = 30, вы знаете, что у железа 30 нейтронов.
- Изотопы атома будут содержать другое количество нейтронов, что изменяет вес атома.
Видео - с помощью этой службы некоторая информация может быть передана YouTube
подсказки
- Цвета могут отличаться, но информация остается прежней.
- Многим людям трудно читать таблицу Менделеева! Не расстраивайтесь, если вы изо всех сил пытаетесь научиться им пользоваться.
- Некоторые периодические таблицы могут упростить информацию. Например, они могут содержать только символ и атомный номер. Подберите стол, который соответствует вашим потребностям.