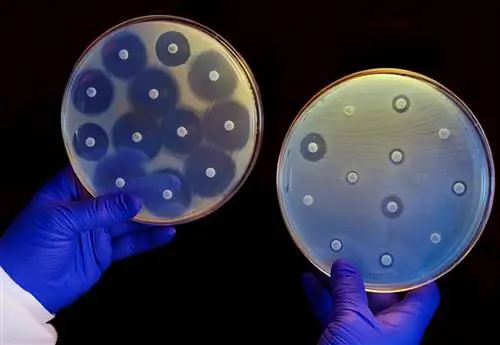
Модель глубокого обучения идентифицирует новый мощный препарат, который может убивать некоторые устойчивые к антибиотикам бактерии.
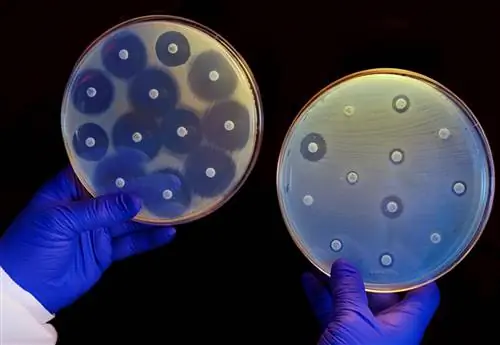
Используя алгоритм машинного обучения, исследователи Массачусетского технологического института идентифицировали новый мощный антибиотик. В лабораторных испытаниях препарат убил многие из самых проблематичных болезнетворных бактерий в мире, в том числе некоторые штаммы, устойчивые ко всем известным антибиотикам. Он также излечил инфекцию у двух разных моделей мышей.
Компьютерная модель, которая может анализировать более ста миллионов химических соединений за несколько дней, предназначена для выбора потенциальных антибиотиков, которые убивают бактерии, используя механизмы, отличные от механизмов существующих лекарств.
«Мы хотели разработать платформу, которая позволила бы нам использовать силу искусственного интеллекта, чтобы открыть новую эру открытия антибиотиков», - говорит Джеймс Коллинз, профессор медицинской инженерии и науки Термеера. в Институте медицинской инженерии и науки Массачусетского технологического института (IMES) и на факультете биологической инженерии. «Наш подход выявил эту удивительную молекулу, которая, возможно, является одним из самых мощных антибиотиков, когда-либо обнаруженных».
В своем новом исследовании исследователи также определили несколько других многообещающих кандидатов в антибиотики, которые они планируют протестировать дальше. Они считают, что модель можно также использовать для разработки новых лекарств, основываясь на том, что она узнала о химических структурах, позволяющих лекарствам убивать бактерии.
«Модель машинного обучения может исследовать in silico большие химические пространства, которые могут быть непомерно дорогими для традиционных экспериментальных подходов», - говорит Регина Барзилай, профессор электротехники и компьютерных наук Delta Electronics в Массачусетском технологическом институте. Лаборатория науки и искусственного интеллекта (CSAIL).
Барзилай и Коллинз, ведущие преподаватели Клиники машинного обучения в здравоохранении имени Абдула Латифа Джамиля Массачусетского технологического института (J-Clinic), являются старшими авторами исследования, опубликованного сегодня в Cell. Первым автором статьи является Джонатан Стоукс, постдоктор Массачусетского технологического института и Института Броуда Массачусетского технологического института и Гарварда.
Новый трубопровод
За последние несколько десятилетий было разработано очень мало новых антибиотиков, и большинство из этих недавно одобренных антибиотиков представляют собой несколько отличающиеся варианты существующих лекарств. Существующие методы скрининга новых антибиотиков часто непомерно дороги, требуют значительных временных затрат и обычно ограничены узким спектром химического разнообразия.
«Мы столкнулись с растущим кризисом, связанным с устойчивостью к антибиотикам, и эта ситуация создается как растущим числом патогенов, становящихся устойчивыми к существующим антибиотикам, так и вялым потоком в биотехнологической и фармацевтической промышленности для новые антибиотики», - говорит Коллинз.
Чтобы попытаться найти совершенно новые соединения, он объединился с Барзилаем, профессором Томми Яаккола и их учениками Кевином Янгом, Кайлом Суонсоном и Венгонгом Джином, которые ранее разработали компьютерные модели машинного обучения, которые могут быть обучены анализировать молекулярные структуры соединений и соотносить их с определенными признаками, такими как способность убивать бактерии.
Идея использования прогностических компьютерных моделей для скрининга «in silico» не нова, но до сих пор эти модели не были достаточно точными, чтобы преобразовать поиск лекарств. Ранее молекулы представлялись в виде векторов, отражающих наличие или отсутствие тех или иных химических групп. Однако новые нейронные сети могут автоматически изучать эти представления, отображая молекулы в непрерывные векторы, которые впоследствии используются для предсказания их свойств.
В этом случае исследователи разработали свою модель для поиска химических особенностей, которые делают молекулы эффективными для уничтожения кишечной палочки.коли. Для этого они натренировали модель примерно на 2500 молекулах, включая около 1700 одобренных FDA лекарств и набор из 800 натуральных продуктов с различной структурой и широким спектром биологической активности..
После того, как модель была обучена, исследователи протестировали ее в Центре перепрофилирования лекарственных средств Института Броуда, библиотеке, содержащей около 6000 соединений. Модель выбрала одну молекулу, которая, как было предсказано, обладала сильной антибактериальной активностью и имела химическую структуру, отличную от любых существующих антибиотиков. Используя другую модель машинного обучения, исследователи также показали, что эта молекула, вероятно, будет иметь низкую токсичность для клеток человека.
Эта молекула, которую исследователи решили назвать галицином, в честь вымышленной системы искусственного интеллекта из «Космической одиссеи 2001 года», ранее исследовалась как возможное лекарство от диабета. Исследователи проверили его на десятках бактериальных штаммов, выделенных от пациентов и выращенных в лабораторных чашках, и обнаружили, что он способен убивать многие из них, устойчивые к лечению, включая Clostridium difficile, Acinetobacter baumannii и Mycobacterium tuberculosis. Препарат работал против всех протестированных видов, за исключением Pseudomonas aeruginosa, трудноизлечимого легочного патогена.
Чтобы проверить эффективность галицина на живых животных, исследователи использовали его для лечения мышей, зараженных A. baumannii, бактерией, которая заразила многих американских солдат, дислоцированных в Ираке и Афганистане. Штамм A. baumannii, который они использовали, устойчив ко всем известным антибиотикам, но применение мази, содержащей галицин, полностью устраняло инфекцию в течение 24 часов.
Предварительные исследования показывают, что галицин убивает бактерии, нарушая их способность поддерживать электрохимический градиент на клеточных мембранах. Этот градиент необходим, помимо других функций, для производства АТФ (молекул, которые клетки используют для хранения энергии), поэтому, если градиент нарушается, клетки умирают. Исследователи говорят, что к такому механизму уничтожения бактериям может быть трудно выработать устойчивость.
«Когда вы имеете дело с молекулой, которая, вероятно, связана с компонентами мембраны, клетка не обязательно может приобрести одну или несколько мутаций, чтобы изменить химический состав внешней мембраны. Подобные мутации, как правило, сложнее приобретать эволюционно», - говорит Стоукс.
В этом исследовании исследователи обнаружили, что E. coli не выработала устойчивости к галицину в течение 30-дневного периода лечения. Напротив, бактерии начали развивать устойчивость к антибиотику ципрофлоксацину в течение одного-трех дней, а через 30 дней бактерии были примерно в 200 раз более устойчивы к ципрофлоксацину, чем в начале эксперимента.
Исследователи планируют продолжить изучение галицина, работая с фармацевтической компанией или некоммерческой организацией, в надежде разработать его для использования на людях.
Оптимизированные молекулы
После идентификации галицина исследователи также использовали свою модель для скрининга более 100 миллионов молекул, выбранных из базы данных ZINC15, онлайн-коллекции из примерно 1 молекулы.5 миллиардов химических соединений. Этот скрининг, который длился всего три дня, выявил 23 кандидата, которые структурно отличались от существующих антибиотиков и, по прогнозам, были нетоксичны для клеток человека.
В лабораторных тестах против пяти видов бактерий исследователи обнаружили, что восемь молекул показали антибактериальную активность, а две из них были особенно мощными. Теперь исследователи планируют продолжить тестирование этих молекул, а также просмотреть больше данных из базы данных ZINC15.
Исследователи также планируют использовать свою модель для разработки новых антибиотиков и оптимизации существующих молекул. Например, они могут научить модель добавлять функции, которые заставят конкретный антибиотик воздействовать только на определенные бактерии, не позволяя ему убивать полезные бактерии в пищеварительном тракте пациента.
«Эта новаторская работа знаменует собой сдвиг парадигмы в открытии антибиотиков и, по сути, в открытии лекарств в целом», - говорит Рой Кишони, профессор биологии и компьютерных наук в Технионе (Израильский технологический институт), который в исследовании не участвовал.«Помимо скрининга кремнезема, этот подход позволит использовать глубокое обучение на всех этапах разработки антибиотиков, от открытия до повышения эффективности и токсичности за счет модификации лекарств и медицинской химии».
Исследование финансировалось Клиникой машинного обучения в здравоохранении имени Абдула Латифа Джамиля, Агентством по снижению угроз обороны, Институтом Броуда, Программой DARPA Make-It, Канадскими институтами медицинских исследований, Канадским Фонд инноваций, Канадская программа научных кафедр, Программа стипендий Бантинга, Научная программа Human Frontier, Фонд Першинг-сквер, Швейцарский национальный научный фонд, Премия Национального института здравоохранения для первых исследователей, Программа стипендий Национального научного фонда для аспирантов, и подарок от Аниты и Джоша Бекенштейнов.
Перепечатано с разрешения MIT News. Прочтите исходную статью.